Estrarre litio dall'acqua di mare? in Arabia Saudita messo a punto un processo sostenibile

Dalla King Abdullah University of Science and Technology (KAUST), Arabia Saudita, un gruppo di ricercatori ha messo a punto un processo per estrarre litio, materiale alla base delle moderne batteria usate in svariati ambiti, utilizzando come elemento di partenza l'acqua di mare
di Carlo Pisani pubblicata il 07 Giugno 2021, alle 08:39 nel canale Scienza e tecnologiaDalla King Abdullah University of Science and Technology (KAUST), Arabia Saudita, un gruppo di ricercatori ha messo a punto un processo per estrarre litio, materiale alla base delle moderne batteria usate in svariate applicazioni, utilizzando come fonte di partenza l'acqua di mare.
Si stima che gli oceani potrebbero contenere circa 5.000 volte più litio che la terra ferma, ma ovviamente in concentrazioni estremamente basse, circa 0,2 parti per milione.
Il team della KAUST ha redatto uno studio, pubblicato sulla rivista Energy & Environmental Science e intitolato "Continuous Electrical Pumping Membrane Process for Seawater Lithium Mining", basandosi su un piccolo impianto di test alimentato a acqua prelevata del Mar Rosso.
Clicca per ingrandire
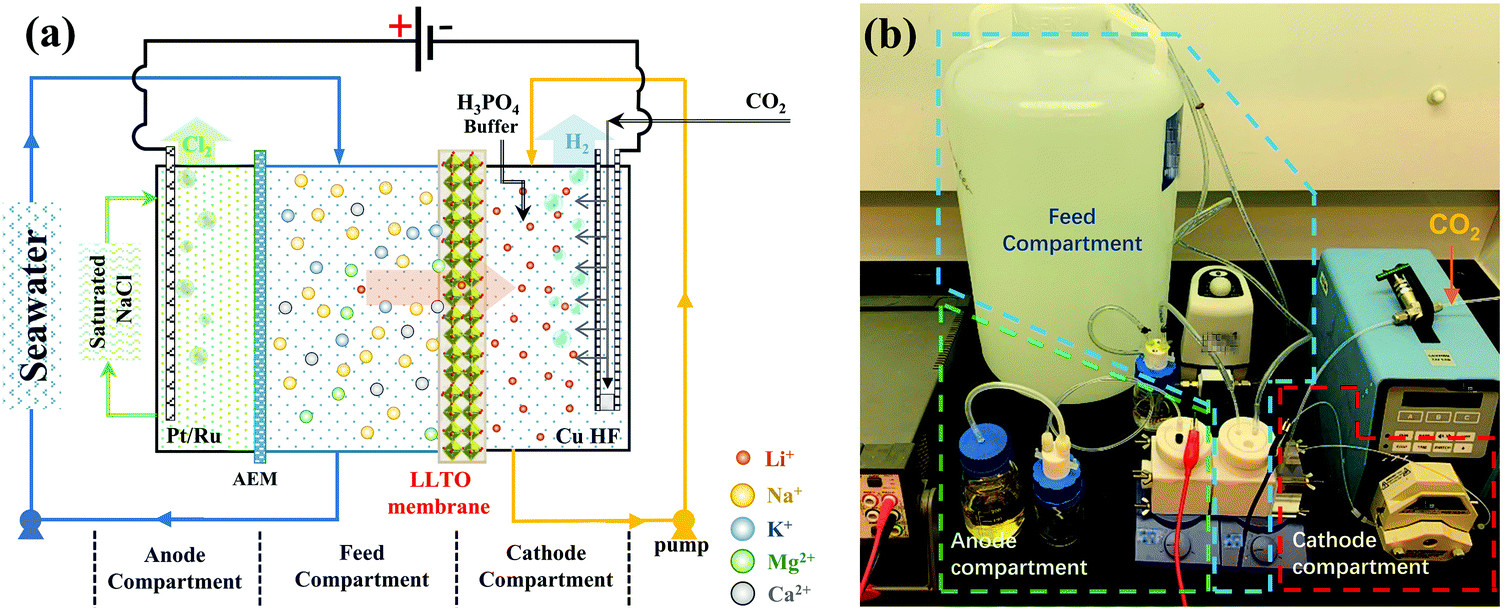
"Il processo di basa su di una cella elettrochimica contenente una membrana ceramica realizzata con ossido di litio, lantanio e titanio (LLTO). La sua struttura cristallina contiene fori abbastanza larghi da consentire il passaggio degli ioni di litio bloccando gli ioni metallici più grandi. La cella contiene tre scomparti.
L'acqua di mare scorre in una camera di alimentazione centrale, dove gli ioni di litio positivi passano attraverso la membrana LLTO in un compartimento laterale che contiene una soluzione tampone e un catodo di rame rivestito di platino e rutenio.
Nel frattempo, gli ioni negativi escono dalla camera di alimentazione attraverso una membrana a scambio anionico standard, passando in un terzo compartimento contenente una soluzione di cloruro di sodio e un anodo di platino-rutenio.
Ad una tensione di 3,25V, la cella genera gas idrogeno al catodo e gas cloro all'anodo. Questo guida il trasporto del litio attraverso la membrana LLTO, dove si accumula nella camera laterale. Quest'acqua arricchita di litio diventa quindi la materia prima per altri quattro cicli di lavorazione, raggiungendo infine una concentrazione di oltre 9.000 ppm. La regolazione del pH di questa soluzione fornisce fosfato di litio solido che contiene semplici tracce di altri ioni metallici, abbastanza puri da soddisfare i requisiti dei produttori di batterie"
Clicca per ingrandire
I ricercatori stimano che la cella avrebbe bisogno di soli 5 $ di elettricità per estrarre 1 kg di litio dalla generica acqua di mare, e il valore dell'idrogeno e del cloro prodotti dalla cella compenserebbe ampiamente tale costo. Inoltre l'acqua di mare residua potrebbe essere utilizzata negli impianti di desalinizzazione per fornire acqua dolce.
"Continueremo a ottimizzare la struttura della membrana e il design delle celle per migliorare l'efficienza del processo" afferma il capo ricercatore Zhiping Lai.
Clicca per ingrandire
Nello studio si indicano delle tempistiche di estrazione ovviamente lunghe, soprattutto per via della tecnologia ancora acerba, ma si precisa che una membrana LLTO potrebbe essere utilizzata per più di 2.000 h mettendo in conto un decadimento di efficacia trascurabile.
Un processo quindi poco affamato di energia, che si basa su un'enorme fonte di approvvigionamento ed in grado di restituire "scarti" riutilizzabili in altri processi, potrebbe essere una valida soluzione per far fronte alla continua crescita della richiesta di litio e quali danni potrebbe comportare all'ecosistema marino?












 La rivoluzione dei dati in tempo reale è in arrivo. Un assaggio a Confluent Current 2025
La rivoluzione dei dati in tempo reale è in arrivo. Un assaggio a Confluent Current 2025 SAP Sapphire 2025: con Joule l'intelligenza artificiale guida app, dati e decisioni
SAP Sapphire 2025: con Joule l'intelligenza artificiale guida app, dati e decisioni Dalle radio a transistor ai Micro LED: il viaggio di Hisense da Qingdao al mondo intero
Dalle radio a transistor ai Micro LED: il viaggio di Hisense da Qingdao al mondo intero Una domenica bestiale Amazon: LG OLED, super portatile Lenovo, iPhone 16 Pro e Pro Max, robot e altri super sconti
Una domenica bestiale Amazon: LG OLED, super portatile Lenovo, iPhone 16 Pro e Pro Max, robot e altri super sconti DJI Mini 4 Pro Fly More Combo: drone leggero che non richiede il patentino oggi in offerta super su Amazon
DJI Mini 4 Pro Fly More Combo: drone leggero che non richiede il patentino oggi in offerta super su Amazon realme GT 7T: display da 6000 nit, potentissimo, 7000 mAh, quasi un top di gamma a metà del prezzo che ti aspetti
realme GT 7T: display da 6000 nit, potentissimo, 7000 mAh, quasi un top di gamma a metà del prezzo che ti aspetti Ancora qualche pezzo per il portatile Lenovo con Core i7, 40GB RAM e 1TB SSD: va sempre a ruba
Ancora qualche pezzo per il portatile Lenovo con Core i7, 40GB RAM e 1TB SSD: va sempre a ruba TV OLED LG Serie C4 2024: immagini da cinema e 4K a 144Hz in sconto su Amazon
TV OLED LG Serie C4 2024: immagini da cinema e 4K a 144Hz in sconto su Amazon Smartwatch Amazfit in sconto: Active 2 a 97, ma ci sono offerte su tutta la gamma
Smartwatch Amazfit in sconto: Active 2 a 97, ma ci sono offerte su tutta la gamma Router e ripetitori AVM FRITZ! da 30 su Amazon: ecco tutte le offerte da non perdere
Router e ripetitori AVM FRITZ! da 30 su Amazon: ecco tutte le offerte da non perdere Adulting 101: i corsi per imparare come era la vita fino a qualche anno fa
Adulting 101: i corsi per imparare come era la vita fino a qualche anno fa Blue Origin ha lanciato con successo la missione suborbitale NS-32 con New Shepard
Blue Origin ha lanciato con successo la missione suborbitale NS-32 con New Shepard L'amministrazione Trump ha ritirato la candidatura di Jared Isaacman come amministratore della NASA
L'amministrazione Trump ha ritirato la candidatura di Jared Isaacman come amministratore della NASA La NASA potrebbe chiudere le missioni OSIRIS-APEX, New Horizons e Juno cancellandone altre per risparmiare soldi
La NASA potrebbe chiudere le missioni OSIRIS-APEX, New Horizons e Juno cancellandone altre per risparmiare soldi Trump vieta anche la vendita di software per la progettazione di chip alle società cinesi
Trump vieta anche la vendita di software per la progettazione di chip alle società cinesi Le migliori offerte del weekend Amazon: portatili, robot, iPhone, Kindle ai prezzi più bassi di sempre
Le migliori offerte del weekend Amazon: portatili, robot, iPhone, Kindle ai prezzi più bassi di sempre Dreame L40 Ultra a 699, prezzo shock: vale quasi quanto lX40 Ultra da 999 (ma costa 300 in meno!)
Dreame L40 Ultra a 699, prezzo shock: vale quasi quanto lX40 Ultra da 999 (ma costa 300 in meno!)



















14 Commenti
Gli autori dei commenti, e non la redazione, sono responsabili dei contenuti da loro inseriti - infoda quel pochissimo che si capisce per un grammo di litio si doverebbe spendere MWh come ridere...
E' anche vero che con la fame di litio a breve costera' piu' dell'argento.
da quel pochissimo che si capisce per un grammo di litio si doverebbe spendere MWh come ridere...
E' anche vero che con la fame di litio a breve costera' piu' dell'argento.
Ehm.... l'articolo parla di 5$ per un Kg di Litio.... la barriera semmai saranno i tempi lunghi, ma come dice l'articolo stesso potrebbe essere messa in testa agli impianti di desalinizzazione producendo:
- litio
- idrogeno
- cloro
- acqua desalinizzata.
Se quanto dichiarato è tutto vero, questa potrebbe diventare la fonte di litio principale negli anni a venire.
Su questo stai sereno che non basterebbero centomila centrali su tutte le coste esistenti sul pianeta.
da quel pochissimo che si capisce per un grammo di litio si doverebbe spendere MWh come ridere...
E' anche vero che con la fame di litio a breve costera' piu' dell'argento.
Nell'articolo originale è indicato questo:
Viene riportato un "Indeed, it was found that the LLTO membrane could be used for >2000 h with a negligible decay in performance."
usando mezza tonnellata di petrolio che in zona costa come la sabbia?
Capisco male è si parla del materiale concentrato a 9000 ppm invece di quello a 0,2 originario?
Da lì a ottenere un KG di Litio ne passa ancora....
Con una concentrazione allo 0,2ppm per avere 1KG di litio puro serve lavorare 5 milioni di Kg di acqua (5 metri cubi più o meno).
Non so se 5 dollari di energia bastano per una quantità d'acqua del genere e non è specificata la velocità di questi processi.
Magari sono 5 dollari ma serve una settimana di lavoro.. quindi servono centinaia se non migliaia di queste camere di estrazione.
Che poi l'acqua liberata dal litio torni al mare o vada ad una desalinatore, credo conti poco.
Viene riportato un "Indeed, it was found that the LLTO membrane could be used for >2000 h with a negligible decay in performance."
Già, sarebbe da capire l'impatto energetico e di riciclo di queste membrane e dei catodi/anodi. 2000h sembrano tante, ma sono 3 mesi di lavoro. Quanti litri di acqua si possono lavorare in queste 2000h?
Se poi funziona per davvero è un'ottima cosa perché ridurrebbe l'impatto delle miniere. Non solo verso l'ambiente, ma anche a verso chi ci lavora.
Il fatto che sia uno studio di ricercatori di quel Paese non implica che quelle tecnologia, se profittevole, debba essere utilizzata solo lì.
Devi effettuare il login per poter commentare
Se non sei ancora registrato, puoi farlo attraverso questo form.
Se sei già registrato e loggato nel sito, puoi inserire il tuo commento.
Si tenga presente quanto letto nel regolamento, nel rispetto del "quieto vivere".